Материалы сайта
Это интересно
Факультет ФНМ МГУ им. М.В.Ломоносова
Химия: Задачи заочного тура 2001 года.
Задача № 1
В 2001 г Факультету Наук о Материалах МГУ им. М.В. Ломоносова исполняется 10 лет. В связи с этим – вопрос с историческим оттенком. Напишите уравнения 10 химических реакций, открытие, изучение и применение которых сыграло, на Ваш взгляд, ключевую роль в развитии химии материалов и способствовало прогрессу человеческого общества. Обоснуйте Ваш выбор. (10 баллов).
Задача № 2
На приведенной схеме каждому символу соответствует индивидуальное вещество, каждой стрелке – уравнение химической реакции.
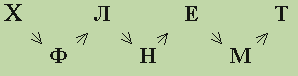
Известен цвет соединений (или растворов): X - бледно-розовый, Ф – фиолетовый, Л – зелёный, Н – коричневый, Е – красно-бурый, М – синий, Т – кирпично-красный. Расшифруйте эту схему, напишите уравнения реакций, укажите условия их проведения. (9 баллов)
Задача № 3
Какие 2 вещества вступили в реакцию, и при каких условиях, если образовались следующие продукты (указаны лишь конечные вещества без стехиометрических коэффициентов):
-> С3H3Cu + NH4Cl + NH3
-> C2H5OH + N2 + NaCl + H2O
-> Na2HPO3 + NaBr
-> ZnSO4 + (NH4)2SO4 + HCl
-> Na2S + CO
(9 баллов)
Задача № 4
Напишите уравнения реакций, соответствующие привёденной схеме. Укажите условия их проведения, для всех веществ приведите графические формулы
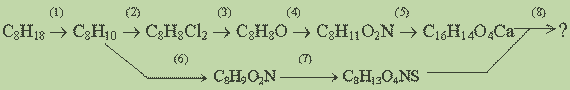
Известно, что в реакции (6) образуется только 1 изомер, а в реакции (2) - 2 изомера. (9 баллов)
Задача № 5
Разделите химическим способом смесь газов, состоящую из метиламина, оксида серы (IV), диоксида углерода и оксида азота (II). Напишите уравнения соответствующих химических реакций. (9 баллов).
Задача № 6
Образец гептагидрата сульфата цинка ZnSO4·7H2O за время хранения частично выветрился с образованием гидратов с меньшим числом воды. 20 г образца растворили в минимально возможном количестве горячей воды при температуре 60 oС, а затем, охладили до 0 oC. При этом выпало 15,08 г чистого гептагидрата ZnSO4·7H2O. Определить состав исходного образца (в массовых процентах). Коэффициент растворимости сульфата цинка при 0 и 60 oC составляет соответственно 42,00 и 75,38. Известно, что наряду с ZnSO4·7H2O существуют ZnSO4·6H2O и ZnSO4·H2O. (9 баллов)
Задача № 7
Сосуд, содержащий 5,98 г тетраоксида диазота N2O4, нагрели до температуры 100 оС. При этом давление внутри сосуда составило 341,1 кПа. Определите константу равновесия реакции разложения N2O4 на газообразный NO2 при 100 оС. Объём сосуда 1 л. (9 баллов)
Задача № 8
При понижении температуры от 20 оС до 5 оС скорость некоторой реакции уменьшилась в 3,5 раза. Чему равен температурный коэффициент и энергия активации этой реакции? (9 баллов)
Задача № 9
В четыре колбы без этикеток налили по 1 л дистиллированной воды и растворили по 1 г следующих солей: Na2SO4·10H2O, AgNO3, Na2CO3, BaCl2. Предложите способ определения содержимого каждой колбы, не прибегая к дополнительным реактивам. Произведения растворимости солей (ПР) AgCl, Ag2SO4, Ag2CO3, BaSO4 и BaCO3 составляют 1,56·10-10, 7,7·10-5, 6,15·10-12, 1,08·10-10, 8,1·10-9 соответственно. Плотности всех растворов считать равными 1 г/мл. (9 баллов)
Задача № 10
Юный химик изучал взаимодействие неизвестного алкена с водным раствором KMnO4. Сначала он провёл реакцию в нейтральной среде и установил, что 5,88 г алкена обесцвечивает 80 мл раствора KMnO4. Затем, он, не меняя количеств алкена и KMnO4, провёл реакцию в растворе горячей конц. H2SO4, причём он заметил, что реакция пошла по другому пути. Химик нейтрализовал полученную смесь избытком K2CO3, выпарил досуха, добавил 3,36 г KOH и сильно прокалил. При этом выделилось 1,12 л газов (н. у.). После некоторых раздумий юному химику удалось объяснить наблюдавшиеся явления и установить формулу алкена. Повторите рассуждения юного химика, напишите соответствующие уравнения реакций, определите, какой алкен был взят, и сколько его изомеров с третичным атомом углерода удовлетворяют условию задачи. (9 баллов)
Задача № 11
Оцените величину теплоты образования связи в молекуле азота, используя следующие данные: теплоты образования газообразных аммиака и гидразина равны 46.2 кДж/моль и -95,4 кДж/моль соответственно, а теплота образования связи N-N в молекуле гидразина составляет 160 кДж/моль. Почему энергии связи в молекулах N2H4 и N2 так сильно различаются? (9 баллов)


