Материалы сайта
Это интересно
Химия
ОСНОВЫ ТЕОРЕТИЧЕСКОЙ ХИМИИ
2. Химические реакции
Закон сохранения массы и энергии. Масса веществ, вступающих в реакцию равна массе веществ, образующихся в результате реакции.
Взаимосвязь массы и энергии выражается уравнением Энштейна:
![]()
где Е – энергия;
m – масса; с – скорость света в вакууме. Закон сохранения массы дает материальную основу для составления уравнений химических реакций и проведения расчетов по ним.Закон постоянства состава. Состав соединений молекулярной структуры, т. е. состоящих из молекул, является постоянным независимо от способа получения. Состав же соединений с немолекулярной структурой (с атомной, ионной и металлической решеткой) не является постоянным и зависит от условий получения.
Стехиометрия. Стехиометрия – раздел химии, в котором рассматриваются массовые и объемные отношения между реагирующими веществами. Стехиометрические количества – количества веществ, которые соответствуют уравнению реакции или формуле. Стехиометрические расчеты – расчеты по химическим формулам или уравнениям, а также вывод формул веществ и уравнений реакций.
Химические превращения. Наличие химических формул для всех веществ позволяет изображать химические реакции посредством химических уравнений. Наиболее характерными признаками химической реакции являются следующие внешние изменения реакционной среды: 1) выделение газа; 2) образование осадка; 3) изменение окраски; 4) выделение или поглощение теплоты.
Тепловые эффекты химических реакций.
Химическая реакция заключается в разрыве одних и образовании других связей, поэтому она сопровождается выделением или поглощением энергии в виде теплоты, света, работы расширения образовавшихся газов.По признаку выделения или поглощения теплоты реакции делятся на экзотермические и эндотермические
.Количество теплоты, которое выделяется или поглощается в результате реакций между определенными
количествами реагентов, называют тепловым эффектом химической реакции и обычно обозначают символом Q.Наряду с тепловым эффектом термохимические процессы очень часто характеризуют разностью энтальпий D H продуктов реакции и исходных веществ.
Энтальпия Н — это определенное свойство вещества, оно является мерой энергии, накапливаемой веществом при его образовании.
Процессы, протекающие при постоянном давлении, встречаются гораздо чаще, чем те, которые протекают при постоянном объеме, так как большинство из них проводится в открытых сосудах. Доказано, что в химических процессах, протекающих при постоянном давлении, выделившееся (или поглощенное) тепло есть мера уменьшения (или соответственно увеличения) энтальпии реакции D H.
При экзотермических реакциях
, когда тепло выделяется, D Н отрицательно. При эндотермических реакциях (тепло поглощается) и D H положительно.Термохимические уравнения. На первых этапах изучения химии вы часто пользовались равным по абсолютной величине и противоположным по знаку обозначением, например:
![]()
где
Q — количество выделенной теплоты. Если использовать энтальпию (характеристику энергосодержания системы), то это уравнение следует записать иначе:![]()
![]()
В справочных таблицах обычно приводят не значения величины
Q, а значения величины D H, измеренные при определенных условиях (чаще всего при 298 К); их обозначают D H0.Теплота образования химических соединений.
Теплотой образования соединения называется количество теплоты, которое выделяется или поглощается при образовании одного моля химического соединения из простых веществ при стандартных условиях (р = 105 Па, T = 298 К). Она измеряется в кДж/моль. Согласно этому определению, теплота образования простого вещества при стандартных условиях равна О.Изменение энтальпии D Н зависит от давления и температуры. Поэтому для того, чтобы облегчить сравнение термохимических данных для различных реакций, были приняты определенные стандартные состояния (условия).
При написании термохимических уравнений твердое вещество, жидкость и газ обязательно обозначаются символами (тв), (ж) и (г) соответственно, поскольку изменение энтальпии зависит от агрегатного состояния реагирующих веществ и продуктов реакции. Стандартное состояние: для газа — состояние чистого газа при
105 Па; для жидкости — состояние чистой жидкости при 105 Па; для твердого вещества — наиболее устойчивое при давлении 105 Па кристаллическое состояние, например графит у углерода, ромбическая сера у серы и т. п. Стандартное состояние всегда относится к 298 К. Так, например, термохимическое уравнение образования воды из водорода и кислорода записывается следующим образом:![]()
Значение 286 кДж является теплотой образования воды в стандартных условиях и означает, что при образовании 1 моля воды выделяется 286 кДж теплоты:
![]()
Отметим, что значение теплоты образования газообразной воды уже будет иным:
![]()
Закон Гесса и его следствия.
Важнейшим законом, на котором основано большинство термохимических расчетов, является закон Гесса (его называют также законом суммы тепловых эффектов).Тепловой эффект химической реакции зависит от состояния исходных веществ и продуктов реакции, но не зависит от промежуточных стадий реакций.
Пример: Тепловой эффект реакции окисления углерода в оксид углерода (IV) не зависит от того, проводится ли это окисление непосредственно:
![]()
или через промежуточную стадию образования оксида углерода (II):
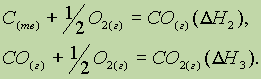
Из закона Гесса следует, что если известны общий тепловой эффект реакции и тепловой эффект одной из двух ее промежуточных стадий, то можно вычислить тепловой эффект
(х) второй промежуточной стадии, т. е. еслиЭто положение очень важно, так как позволяет рассчитывать тепловые эффекты для реакций, не поддающихся непосредственному экспериментальному изучению.
Если теплота образования какого-либо вещества из простых веществ не измерена экспериментально, то для расчета можно воспользоваться значениями D Н ряда других соединений; комбинируя эти значения, можно получить D Нобр искомого соединения.
Особенно удобно проводить такие расчеты, используя следствия, непосредственно вытекающие из закона Гесса:
Тепловой эффект химической реакции равен разности суммы теплот образования продуктов реакции
и суммы теплот образования исходных веществ (суммирование проводится с учетом числа молей веществ, участвующих в реакции, т. е. стехиометрических коэффициентов в уравнении протекающей реакции):![]()
Здесь
Qi, Qj — теплоты образования продуктов реакции и исходных веществ соответственно; ni, и nj — стехиометрические коэффициенты в правой и левой частях термохимического уравнения соответственно.Аналогичным образом можно записать:
![]()
где D н — изменение энтальпии соответствующей реакции,D
Hi, D Hj— энтальпии образования продуктов реакции и исходных веществ соответственно.Химическая кинетика
трактует качественные и количественные изменения в ходе химического процесса, происходящие во времени. Обычно эту общую задачу подразделяют на две более конкретные:1)
выявление механизма реакции — установление элементарных стадий процесса и последовательности их протекания (качественные изменения);2)
количественное описание химической реакции — установление строгих соотношений, которые могли бы удовлетворительно предсказывать изменения количеств исходных реагентов и продуктов по мере протекания реакции.Как правило, химическая реакция протекает в несколько промежуточных стадий, которые, складываясь, дают суммарную реакцию.
Элементарная стадия реакции. Кинетическое уравнение химической реакции (с учетом механизма реакции) может быть получено только в результате экспериментального изучения реакции и не может быть выведено из стехиометрического уравнения суммарной реакции. При обсуждении механизмов реакций принято различать реакции по их молекулярности
, т. е. по числу молекул, участвующих в каждом элементарном акте взаимодействия. По этому признаку различают реакции мономолекулярные, бимолекулярные и тримолекулярные.Мономолекулярными
называются реакции, в которых элементарный акт представляет собой химическое превращение одной молекулы, которое в общем виде можно описать уравнениемА = В + С.
Бимолекулярные
— это такие реакции, элементарный акт в которых осуществляется при столкновении двух молекулА + В = С.
В тримолекулярных
реакциях элементарный акт осуществляется при одновременном столкновении трех молекул2А + В = С.
Столкновение более чем трех молекул одновременно практически невероятно, поэтому реакции большей молекулярности на практике не обнаружены.
Скорость химической реакции.
Основным понятием в химической кинетике является, понятие о скорости реакции:Скорость химической реакции определяется количеством вещества, прореагировавшего в единицу времени в единице объема.
Если при неизменных объеме и температуре концентрация одного из реагирующих веществ уменьшилась от с
1 до с2 за промежуток времени от t1 до t2, то в соответствии с определением скорость реакции за данный промежуток времени равна:![]()
Знак “-” в правой части уравнения появляется т. к. по мере протекания реакции (
t2-t1 > 0) концентрация реагентов убывает, следовательно, c2-c1 < О, а так как скорость реакции всегда положительна, то перед дробью следует поставить знак “-”.Обычно для реакций, протекающих в газах или растворах, концентрации реагентов выражают в моль/л, а скорость реакции — в моль/(л× с).
Скорость каждой химической реакции зависит как от природы реагирующих веществ, так и от условий, в которых реакция протекает. Важнейшими из этих условий являются: концентрация, температура и присутствие катализатора. Природа реагирующих веществ оказывает решающее влияние на скорость химической реакции. Так, например, водород с фтором реагирует очень энергично уже при комнатной температуре, тогда как с бромом значительно медленнее даже при нагревании.
Зависимость скорости гомогенных реакций от концентрации (закон действующих масс).
Влияние концентрации реагирующих веществ может быть объяснено из представлений, согласно которым химическое взаимодействие является результатом столкновения частиц. Увеличение числа частиц в заданном объеме приводит к более частым их столкновениям, т. е. к увеличению скорости реакции.Количественно зависимость между скоростью реакции и молярными концентрациями реагирующих веществ описывается основным законом химической кинетики — законом действующих масс.
Скорость химической реакции при постоянной температуре прямо пропорциональна произведению концентраций реагирующих веществ.
Для мономолекулярной реакции скорость реакции u
определяется концентрацией молекул вещества А:![]()
где
k — коэффициент пропорциональности, который называется константой скорости реакции; [А] — молярная концентрация вещества А.В случае бимолекулярной реакции, ее скорость определяется концентрацией молекул не только вещества А, но и вещества В:
![]()
В случае тримолекулярной реакции,
скорость реакции выражается уравнением:![]()
В общем случае, если в реакцию вступают одновременно т молекул вещества А и
n молекул вещества В, т. е.тА + пВ = С
,уравнение скорости реакции имеет вид:
![]()
Это уравнение есть математическое выражение закона действующих масс в общем виде.
Чтобы понять физический смысл константы скорости реакции, надо принять в написанных выше уравнениях, что [А] = 1 моль/л и [В] = 1 моль/л (либо приравнять единице их произведение), и тогда u = k. Отсюда ясно, что константа скорости k численно равна скорости реакции, когда концентрации реагирующих веществ (или их произведение в уравнениях скорости) равны единице.
Общее выражение для скорости химической реакции получено для данной, фиксированной температуры. В общем же случае, поскольку скорость реакции зависит от температуры, закон действующих масс записывается как
![]()
где u и
k являются функциями температуры.Гомогенные и гетерогенные реакции.
Приведенная выше зависимость скорости химической реакции от концентрации реагирующих веществ справедлива для газов и реакций, протекающих в растворах. Она не распространяется на реакции с участием твердых веществ, так как в этих случаях взаимодействие молекул происходит не во всем объеме реагирующих веществ, а лишь на поверхности, от размера которой также зависит скорость реакции. Поэтому реакции в гетерогенных системах протекают значительно сложнее.Гетерогенной
называется система, состоящая из отдельных частиц, находящихся в различных агрегатных состояниях и разграниченных между собой определенными поверхностями раздела. Отдельные однородные части гетерогенной системы называются ее фазами.Пример:
при 0 °С лед, вода и находящийся над ними пар образуют гетерогенную систему из трех фаз: твердой — льда, жидкой — воды и газообразной — водяного пара; кислота и реагирующие с нею кусочки металла образуют систему из трех фаз и т. д.В гетерогенной системе реакция всегда происходит на поверхности раздела двух фаз, так как только здесь молекулы различных фаз могут сталкиваться между собой. Поэтому скорость гетерогенной реакции зависит не только от рассмотренных ранее факторов, но и от величины поверхности соприкосновения между реагирующими фазами. Всякое увеличение поверхности приводит и к увеличению скорости реакции. Например, растворение металлов в кислотах протекает намного быстрее, если брать металлы в виде порошков.
Константа скорости химической реакции, ее зависимость от температуры. Многочисленные опыты показывают, что при повышении температуры скорость большинства химических реакций существенно увеличивается, причем для реакций в гомогенных системах при нагревании на каждые десять градусов скорость реакции возрастает в 2—
4 раза (правило Вант-Гоффа).Это правило связано с понятием температурного коэффициента скорости реакции g и определяется соотношением
![]()
При температурах, не очень значительно изменяющихся, для многих реакций в соответствии с правилом
Вант-Гоффа g
= 2 ¸ 4.Значение температурного коэффициента g дает возможность рассчитать изменение скорости реакции при увеличении температуры на некоторое число градусов от Т
1 до Т2 по формуле![]()
Очевидно, что при повышении температуры в арифметической прогрессии скорость реакции возрастает в геометрической.
Энергия активации. С. Аррениус впервые показал, что влияние температуры сводится к увеличению числа активных молекул, т. е. таких молекул, которые в момент столкновения обладают энергией, не меньше определенной для данной реакции величины, называемой энергией активации химической реакции.
Энергия активации — это некоторое избыточное количество энергии (по сравнению со средней), необходимое для вступления молекул в реакцию.
Согласно Аррениусу, константа скорости химической реакции зависит от температуры экспоненциально:
![]()
Здесь Е — энергия активации (Дж/моль),
R — универсальная газовая постоянная, T — температура в К,А — константа.
Явление катализа. Одно из наиболее сильных средств воздействия на скорость химических реакций — использование катализаторов.
Катализаторы. Катализатором называется вещество, изменяющее скорость химической реакции, но остающееся неизменным после того, как химическая реакция заканчивается.
Влияние катализаторов на скорость реакции называется катализом. Когда взаимодействующие вещества и катализатор находятся в одном агрегатном состоянии, говорят о гомогенном катализе. При гетерогенном катализе реагирующие вещества и катализатор находятся в различных агрегатных состояниях: обычно катализатор — в твердом, а реагирующие вещества — в жидком или газообразном (пример: в случае окисления
SO2 в SO3 в присутствии платины или оксида ванадия (V) происходит гетерогенный катализ).О механизмах гомогенного и гетерогенного катализа. Механизм действия катализаторов может быть самым разнообразным и, как правило, очень сложным. Основной гипотезой, объясняющей влияние катализатора на скорость реакции, является предположение об образовании промежуточных продуктов при взаимодействии катализатора и реагирующего вещества. Если химическая реакция А + В = АВ без катализатора происходит медленно, а в присутствии катализатора К быстро, то его действие объясняется тем, что катализатор реагирует с одним из исходных веществ, образуя непрочное (как правило, очень реакционноспособное) промежуточное соединение АК (или
ВК):А (В) + К = АК (ВК).
Образовавшееся промежуточное соединение (например.
АК) взаимодействует с другим исходным веществом В, образуя конечный продукт реакции АВ и выделяя катализатор К в первоначальном виде:АК + В = АВ + К.
Приведенная простейшая схема катализа ясно показывает, почему каждая частица катализатора может принимать участие в реакции бесчисленное множество раз. (Правда, “бесчисленное” - только теоретически, потому что практически некоторые вещества, даже в очень малых количествах, могут резко снижать скорость каталитической реакции, уменьшая или полностью уничтожая активность катализатора. Такие вещества называют каталитическими ядами, а само явление снижения активности катализатора - отравлением.) Отсюда ясно, почему катализатор после окончания реакции остается количественно и химически неизменным.
Обратимые реакции. В химических реакциях исходные вещества не всегда полностью превращаются в продукты реакции. Это происходит потому, что по мере накопления продуктов реакции могут создаваться условия для протекания обратимой реакции в противоположном направлении.
Например, если смешать пары иода с водородом при температуре 200
°С, то произойдет реакция:![]()
Однако известно, что йодистый водород уже при нагревании до 180 °С начинает разлагаться на иод и водород:
![]()
Понятно, что в этих условиях не произойдет ни полного разложения Н
I, так как продукты реакции способны вновь реагировать между собой, ни полного образования йодистого водорода. Химические реакции, которые при одних и тех же условиях могут идти в противоположных направлениях. называются обратимыми.При написании уравнений обратимых реакций вместо знака равенства ставят две противоположно направленные стрелки. Уравнение рассмотренной выше обратимой реакции запишется следующим образом:
![]()
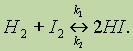
Реакцию, протекающую слева направо называют прямой (константа скорости прямой реакции
k1), справа налево — обратной (константа скорости обратной реакции k2).Химическое равновесие.
В обратимых реакциях скорость прямой реакции вначале имеет максимальное значение, а затем уменьшается вследствие уменьшения концентрации исходных веществ, расходуемых на образование продуктов реакции. И наоборот, обратная реация в начальный момент имеет минимальную скорость, которая увеличивается по мере увеличения концентрации продуктов реакции. Следовательно, скорость прямой реакции уменьшается, а обратной — увеличивается. Наконец, наступает такой момент, когда скорости прямой и обратной реакций становятся равными.Состояние, в котором скорость обратной реакции становится равной скорости прямой реакции, называется химическим равновесием.
Константа равновесия, степень превращения. Состояние химического равновесия обратимых процессов количественно характеризуется константой равновесия. Так, для обратимой реакции, которую в общем виде можно записать как
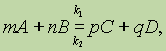
согласно закону действующих масс, скорости прямой реакции u
1 и обратной u 2 соответственно запишутся следующим образом: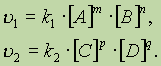
В момент достижения состояния химического равновесия скорости прямой и обратной реакций равны:
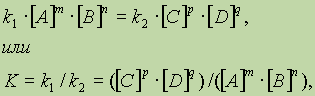
где К — константа равновесия, представляющая собой отношение констант скорости прямой и обратной
реакций.
В правой части первого уравнения стоят те концентрации взаимодействующих веществ, которые устанавливаются при равновесии, — равновесные концентрации.
Второе уравнение
представляет собой математическое выражение закона действующих масс при химическом равновесии.Этот закон является одним из наиболее важных в химии.
Исходя из кинетического уравнения любой химической реакции, можно сразу же записать отношение, связывающее равновесные концентрации реагирующих веществ и продуктов реакции. Если определить константу К экспериментально, измеряя равновесные концентрации всех веществ при данной температуре, то полученное значение можно использовать в расчетах для других случаев равновесия при той же температуре.Численное значение константы равновесия характеризует тенденцию к осуществлению реакции или, другими словами, характеризует выход данной реакции. Так, при К >> 1 выход реакции велик, так как при этом
![]()
Понятно, что при К
<< 1 выход реакции мал.Принцип Ле Шателье. Состояние химического равновесия при неизменных внешних условиях может сохраняться сколь угодно долго. В действительности же реальные системы обычно испытывают различные воздействия (изменение температуры, давления или концентрации реагентов), выводящие систему из состояния равновесия. Как только в системе нарушается равновесие, скорости прямой и обратной становятся неодинаковыми и в системе преимущественно протекает процесс, который приводит ее к состоянию равновесия, но уже отвечающему новым условиям. Изменения, происходящие в системе в результате внешних воздействий, определяются принципом подвижного равновесия — принципом Ле Шателье.
Внешнее воздействие на систему, находящуюся в состоянии равновесия, приводит к смещению этого равновесия в направлении, при котором эффект произведенного воздействия ослабляется.
Внешнее воздействие на систему изменяет соотношение между скоростями прямого и обратного процесса, благоприятствуя тому из них, который противодействует внешнему влиянию.
Принцип Ле Шателье универсален, так как применим не только к чисто химическим процессам, но и к физико-химическим явлениям, таким, как кристаллизация, растворение, кипение, фазовые превращения в твердых телах.
Смещение химического равновесия под действием температуры и давления (концентрации).
Концентрация. Увеличение концентрации одного из реагирующих веществ сначала приводит к увеличению числа молекул этого вещества. Поскольку число столкновений с участием этих молекул увеличивается, реакция, для которой они являются реагентами, ускоряется. Это приводит к увеличению концентраций реагентов у противоположной реакции и т. д. В результате изменяется концентрация всех веществ, участвующих в химической реакции.Можно сделать вывод, что при увеличении концентрации одного из реагирующих веществ равновесие смещается в сторону расхода этого вещества, при уменьшении концентрации равновесие смещается в сторону образования этого вещества.
Давление. Влияние давления очень напоминает эффект изменения концентраций реагирующих веществ, но сказывается оно практически только на газовых системах. При повышении давления увеличивается число молекул в единице объема газовой системы. Прямая или обратная реакция, в которой участвует большее количество газообразных веществ, протекает при этом с большей скоростью. В результате этой реакции образуется больше молекул тех веществ, которые участвуют в обратной реакции. Произойдет изменение скорости обратной реакции, и в конце концов будет достигнуто новое состояние равновесия.
При увеличении давления равновесие смещается в сторону уменьшения числа молекул газообразных веществ, т. е. в сторону понижения давления: при уменьшении давления равновесие смещается в сторону возрастания числа молекул газообразных веществ, т. е. в сторону увеличения давления. Если реакция протекает без изменения числа молекул газообразных веществ, то давление не влияет на положение равновесия в этой системе.
Температура. Повышение температуры увеличивает кинетическую энергию всех молекул, участвующих в реакции. Но молекулы, вступающие в реакцию, при которой происходит поглощение энергии (эндотермическая реакция), начинают взаимодействовать между собой быстрее. Это увеличивает концентрацию молекул, участвующих в обратной реакции, и ускоряет ее. В результате достигается новое состояние равновесия с повышенным содержанием продуктов реакции, протекающей с поглощением энергии.
При повышении температуры равновесие смещается в сторону эндотермической реакции, при понижении температуры — в сторону экзотермической реакции.


