Материалы сайта
Это интересно
Факультет ФНМ МГУ им. М.В.Ломоносова
Химия: Задачи заочного тура 2000 года.
Задача № 1
Путем химических превращений, используя катализаторы, из воды и двух простых веществ, выбранных Вами, получите 8 веществ, относящихся к различным классам органических и неорганических соединений, из которых 4 вещества имеют одинаковый качественный элементный состав.(10 баллов).
Задача № 2
На приведенной схеме каждой букве соответствует индивидуальное вещество, содержащее один и тот же элемент, каждой стрелке - уравнение химической реакции с участием этого вещества и любых других веществ.
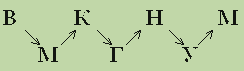
Известно, что все реакции являются окислительно - восстановительными, а вещество В - простое. Расшифруйте эту схему, напишите уравнения реакций, укажите условия их проведения. (10 баллов).
Задача № 3
Какие вещества вступили в реакцию и при каких условиях, если образовались следующие продукты (указаны лишь конечные вещества без стехиометрических коэффициентов):
-> Al(OH)3 + CO2 + NaCl
-> FeCl2 + CuCl2
-> CCl4 + HCl
-> C6H5OH + CH3COCH3
-> CH3COOH +CO2 +MnSO4 +K2SO4 +H2O
(10 баллов)
Задача № 4
Напишите уравнения реакций, соответствующие привёденной схеме. Укажите условия их проведения:
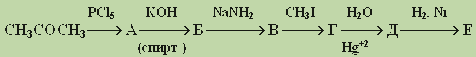
(10 баллов)
Задача № 5
В 1992 г взаимодействием Rb2O с RbNO3 был получен ортонитрат рубидия Rb3NO4.
1) Предскажите, как это соединение будет реагировать с водным раствором ZnCl2.
2) Изобразите графические формулы кислот HNO2, HNO3, Н3NO4. Укажите валентность, степень окисления и тип гибридизации атомов N в каждом из этих соединений.
3) Расположите эти соединения в порядке возрастания а) устойчивости, б) кислотных свойств, в) окислительных свойств. Приведите по 2 химических реакции, характеризующие ваш выбор. (10 баллов)
Задача № 6
Смесь сульфидов FeS2, ZnS, Cu2S подвергли обжигу в избытке кислорода. При этом масса смеси уменьшилась на 12 г и выделилось 80 л SO2 (объём газа измерен при температуре 702 градуса C и давлении 1,5 атм.). Сколько литров CO выделится при нагревании обожжёной смеси с избытком углерода при температуре 900 С и давлении 823 мм. рт. ст.? Какова максимально возможная масса исходной смеси ? (15 баллов)
Задача № 7
При нагревании вещества "A" C3H7O2N в присутствии катализатора образуется легкополимеризующееся вещество C3H3N, при взаимодействии "А" с водным раствором HCl образуется C3H5O2Cl, с гидрооксидом кальция - C6H6O4Ca. Напишите графические формулы указанных веществ и уравнения реакций, упомянутых в задаче. (10 баллов)
Задача № 8
Через два соединённых параллельно электролизёра, содержащих водные растворы NaCl и Ca(NO3)2 и имеющих сопротивления R1 и R2 соответственно, в течение некоторого времени пропускали постоянный электрический ток. Все газы, выделившиеся в электролизёрах, собрали вместе и нагрели. При этом после охлаждения образовался 33,64 % (масс.) раствор HCl массой m1. Оказалось, что если электролизёры с исходными растворами соединить последовательно и в течение некоторого времени собирать все выделяющиеся в ходе электролиза газы, то после их нагревания можно получить раствор HCl массой m2 (m1 не равно m2) той же самой концентрации. Определить величину R1/R2. Изменением значений R1 и R2 в ходе электролиза пренебречь. (15 баллов)
Задача № 9
Оцените энергию связи C-C в алмазе, учитывая, что каждый атом углерода окружён четыремя другими, расположенными по отношению к нему в вершинах тетраэдра. В среднем на один атом C приходится 2 связи. Для расчета используйте следующие данные: теплота сгорания графита 393,51 кДж/моль, теплота сгорания алмаза 395,34 кДж/моль, теплота сублимации графита -717 кДж/моль. Как объяснить необычайно высокую прочность алмаза по сравнению с другими аллотропными модификациями углерода? (10 баллов)


